Nat Med | Mitmeoomiline lähenemine kolorektaalse vähi integreeritud kasvaja-, immuun- ja mikroobimaastiku kaardistamisele paljastab mikrobiomi interaktsiooni immuunsüsteemiga
Kuigi primaarse käärsoolevähi biomarkereid on viimastel aastatel põhjalikult uuritud, tuginevad praegused kliinilised juhised ravisoovituste määramisel ainult kasvaja-lümfisõlmede-metastaaside staadiumi määramisele ja DNA mittevastavuse parandamise (MMR) defektide või mikrosatelliidi ebastabiilsuse (MSI) tuvastamisele (lisaks standardsele patoloogilisele testimisele). Teadlased on täheldanud seose puudumist geeniekspressioonil põhinevate immuunvastuste, mikroobide profiilide ja kasvaja stroomi vahel vähi genoomi atlase (TCGA) kolorektaalvähi kohordis ning patsientide elulemuse vahel.
Uuringute edenedes on teatatud, et primaarse kolorektaalse vähi kvantitatiivsed omadused, sealhulgas vähi rakuline, immuunne, stromaalne või mikroobne olemus, korreleeruvad oluliselt kliiniliste tulemustega, kuid arusaam sellest, kuidas nende koostoimed mõjutavad patsientide tulemusi, on endiselt piiratud.
Fenotüübilise keerukuse ja tulemuse vahelise seose analüüsimiseks töötas Katari Sidra Meditsiiniuuringute Instituudi teadlaste meeskond hiljuti välja ja valideeris integreeritud skoori (mICRoScore), mis tuvastab hea ellujäämismääraga patsientide rühma, kombineerides mikrobioomi omadusi ja immuunsüsteemi hülgamiskonstante (ICR). Meeskond viis läbi 348 primaarse kolorektaalvähiga patsiendi värskelt külmutatud proovide põhjaliku genoomse analüüsi, mis hõlmas kasvajate ja sobitatud tervete kolorektaalsete kudede RNA sekveneerimist, kogu eksoomi sekveneerimist, sügava T-rakkude retseptori ja 16S bakteriaalse rRNA geeni sekveneerimist, mida täiendati kogu kasvaja genoomi sekveneerimisega mikrobioomi täpsemaks iseloomustamiseks. Uuring avaldati ajakirjas Nature Medicine pealkirjaga „Kolorektaalvähi integreeritud kasvaja, immuunsüsteemi ja mikrobioomi atlas“.

Artikkel avaldatud ajakirjas Nature Medicine
AC-ICAM-i ülevaade
Teadlased kasutasid ortogonaalset genoomilist platvormi värskelt külmutatud kasvajaproovide analüüsimiseks ja kõrvuti asetsevate tervete käärsoolekoeproovide (kasvaja-normaalne paari) sobitamiseks patsientidelt, kellel oli histoloogiliselt diagnoositud käärsoolevähk ilma süsteemse ravita. Tuginedes kogu eksoomi sekveneerimisele (WES), RNA-seq andmete kvaliteedikontrollile ja kaasamiskriteeriumide sõelumisele, säilitati 348 patsiendi genoomilised andmed ja kasutati neid järgnevas analüüsis keskmise jälgimisajaga 4,6 aastat. Uurimisrühm nimetas selle ressursi Sidra-LUMC AC-ICAM: Kaart ja juhend immuunsüsteemi, vähi ja mikrobioomi interaktsioonide kohta (joonis 1).
Molekulaarne klassifikatsioon ICR-i abil
Uurimisrühm jäädvustas pideva vähi immunoseire jaoks modulaarse immuungeneetiliste markerite komplekti, mida nimetatakse hülgamisreaktsiooni immuunkonstandiks (ICR), ning optimeeris ICR-i, koondades selle 20-geeniliseks paneeliks, mis hõlmab erinevaid vähiliike, sealhulgas melanoomi, põievähki ja rinnavähki. ICR-i on seostatud ka immunoteraapia vastusega mitmesuguste vähiliikide, sealhulgas rinnavähi korral.
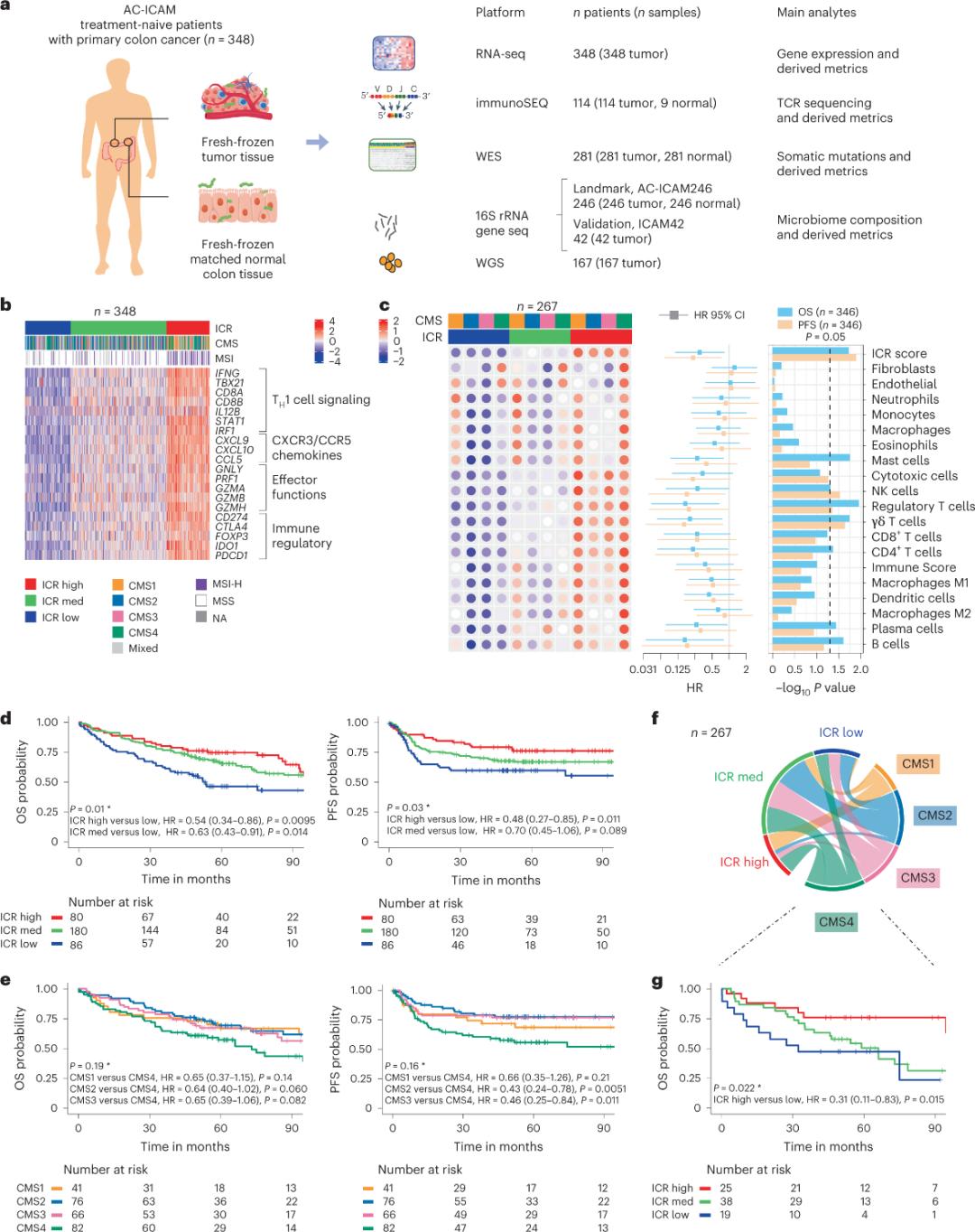
Esiteks valideerisid teadlased AC-ICAM kohordi ICR-i signatuuri, kasutades ICR-i geenipõhist kaasklassifikatsiooni lähenemisviisi, et liigitada kohordi kolme klastrisse/immuunsüsteemi alatüüpi: kõrge ICR (kuumad kasvajad), keskmine ICR ja madal ICR (külmad kasvajad) (joonis 1b). Teadlased iseloomustasid immuunkalduvust, mis on seotud konsensusmolekulaarsete alatüüpidega (CMS), mis on transkriptoomil põhinev käärsoolevähi klassifikatsioon. CMS-i kategooriate hulka kuulusid CMS1/immuunne, CMS2/kanooniline, CMS3/metaboolne ja CMS4/mesenhümaalne. Analüüs näitas, et ICR-i skoorid olid negatiivses korrelatsioonis teatud vähirakkude radadega kõigis CMS-i alatüüpides ning positiivseid korrelatsioone immunosupressiivsete ja stroomaga seotud radadega täheldati ainult CMS4 kasvajate puhul.
Kõigis krooniliselt metaboolsetes metaboliseeritavates patsientides oli looduslike tapjarakkude (NK) ja T-rakkude alamhulkade arvukus suurim ICR-i kõrge immuunsusega alatüüpides, kusjuures teiste leukotsüütide alamhulkade puhul oli varieeruvus suurem (joonis 1c). ICR-i immuunalatüüpidel oli erinev üldine elulemus (OS) ja progresseerumisvaba elulemus (PFS), kusjuures ICR suurenes järk-järgult madalast kõrgeni (joonis 1d), mis kinnitab ICR-i prognostilist rolli kolorektaalvähi korral.
Joonis 1. AC-ICAM uuringu ülesehitus, immuunsüsteemiga seotud geenisignatuur, immuun- ja molekulaarsed alatüübid ning ellujäämine.
ICR püüab kinni kasvajaga rikastatud, klooniliselt amplifitseeritud T-rakud
Ainult väike osa kasvajakoesse infiltreeruvatest T-rakkudest on teatatud olevat spetsiifilised kasvaja antigeenide suhtes (alla 10%). Seetõttu nimetatakse enamikku kasvajasiseseid T-rakke kõrvalseisjateks T-rakkudeks (bystander T-rakud). Kõige tugevam korrelatsioon produktiivsete T-rakkudega tavapäraste T-rakkude arvuga täheldati stroomarakkude ja leukotsüütide alampopulatsioonides (tuvastatud RNA-seq abil), mida saab kasutada T-rakkude alampopulatsioonide hindamiseks (joonis 2a). ICR-klastrites (üldine ja CMS-klassifikatsioon) täheldati immuun-SEQ TCR-ide kõrgeimat klonaalsust ICR-kõrge ja CMS-alatüübi CMS1/immuunrühmades (joonis 2c), kus ICR-kõrgete kasvajate osakaal oli suurim. Kasutades kogu transkriptoomi (18 270 geeni), olid kuus ICR-geeni (IFNG, STAT1, IRF1, CCL5, GZMA ja CXCL10) kümne TCR-i immuun-SEQ klonaalsusega positiivselt seotud geeni hulgas (joonis 2d). ImmunoSEQ TCR-i klonaalsus korreleerus enamiku ICR-i geenidega tugevamalt kui kasvajale reageerivate CD8+ markerite abil täheldatud korrelatsioonid (joonis 2f ja 2g). Kokkuvõtteks võib öelda, et ülaltoodud analüüs viitab sellele, et ICR-i signatuur kajastab kasvajaga rikastatud, klonaalselt amplifitseeritud T-rakkude olemasolu ja võib selgitada selle prognostilist tähtsust.
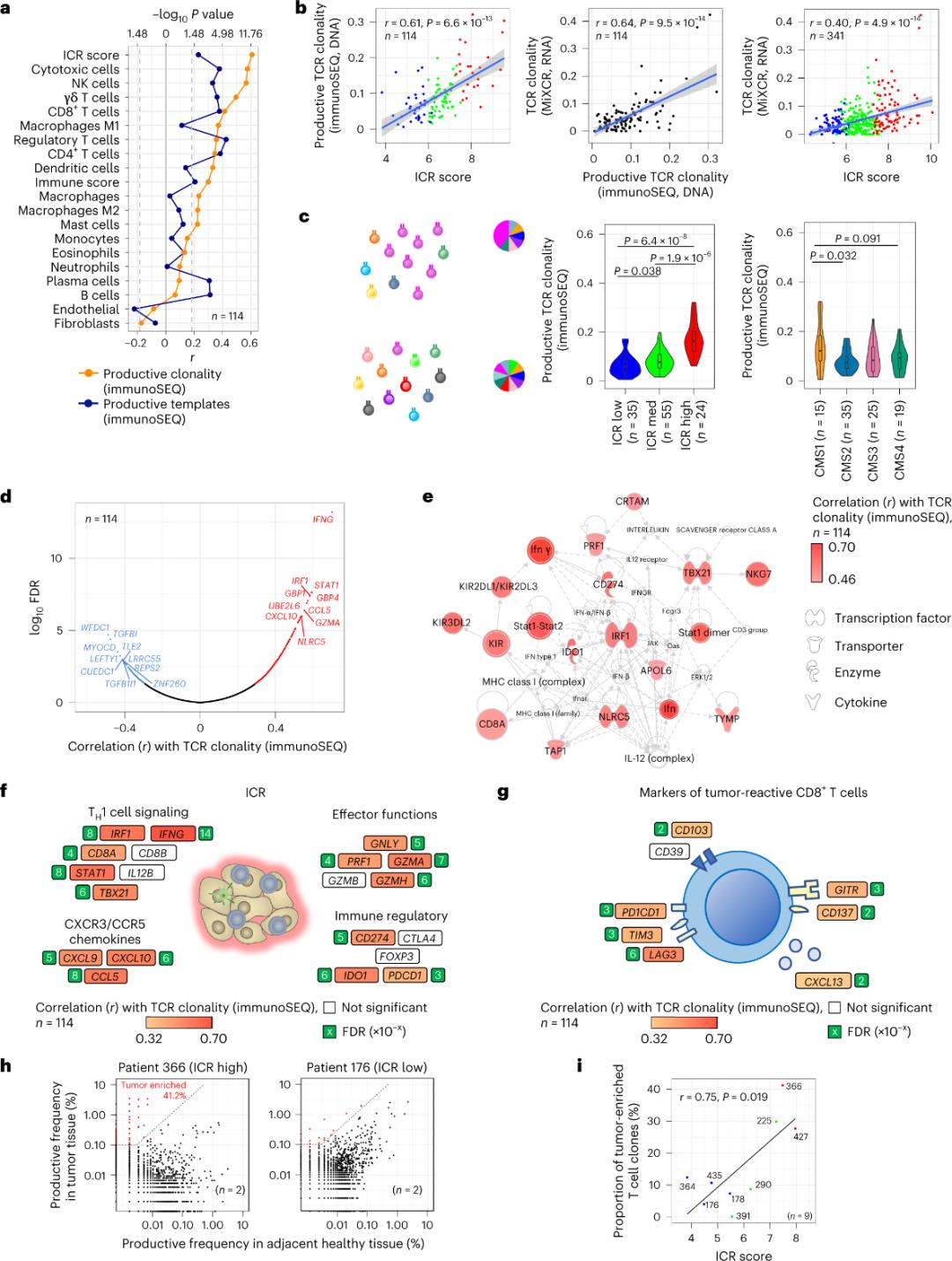
Joonis 2. TCR-i mõõdikud ja korrelatsioon immuunsusega seotud geenide, immuunsuse ja molekulaarsete alatüüpidega.
Mikrobioomi koostis tervetes ja käärsoolevähi kudedes
Teadlased viisid läbi 16S rRNA sekveneerimise, kasutades 246 patsiendilt saadud sobitatud kasvaja ja terve käärsoolekoe DNA-d (joonis 3a). Valideerimiseks analüüsisid teadlased lisaks 16S rRNA geeni sekveneerimise andmeid veel 42 kasvajaproovist, millel puudus analüüsiks sobiv normaalne DNA. Esiteks võrdlesid teadlased sobitatud kasvajate ja terve käärsoolekoe floora suhtelist arvukust. Clostridium perfringens oli kasvajates oluliselt suurem võrreldes tervete proovidega (joonis 3a-3d). Kasvaja ja tervete proovide vahel ei täheldatud alfa-mitmekesisuses (liikide mitmekesisus ja arvukus ühes proovis) olulist erinevust ning ICR-kõrge kasvajate puhul täheldati mikroobide mitmekesisuse tagasihoidlikku vähenemist võrreldes ICR-madala kasvajatega.
Mikroobide profiilide ja kliiniliste tulemuste vaheliste kliiniliselt oluliste seoste tuvastamiseks seadsid teadlased eesmärgiks kasutada 16S rRNA geeni sekveneerimise andmeid, et tuvastada ellujäämist ennustavaid mikrobioomi tunnuseid. AC-ICAM246 uuringus käivitasid teadlased OS Coxi regressioonimudeli, mis valis välja 41 nullist erinevate koefitsientidega tunnust (mis on seotud diferentsiaalse suremuse riskiga) ja mida nimetatakse MBR klassifikaatoriteks (joonis 3f).
Selles treeningkohordis (ICAM246) seostati madalat MBR-skoori (MBR<0, madal MBR) oluliselt madalama surmariskiga (85%). Teadlased kinnitasid seost madala MBR-i (riski) ja pikema üldise elulemuse vahel kahes sõltumatult valideeritud kohordis (ICAM42 ja TCGA-COAD). (Joonis 3) Uuring näitas tugevat korrelatsiooni endogastriliste kokkide ja MBR-skooride vahel, mis olid kasvaja ja terve käärsoolekoe puhul sarnased.
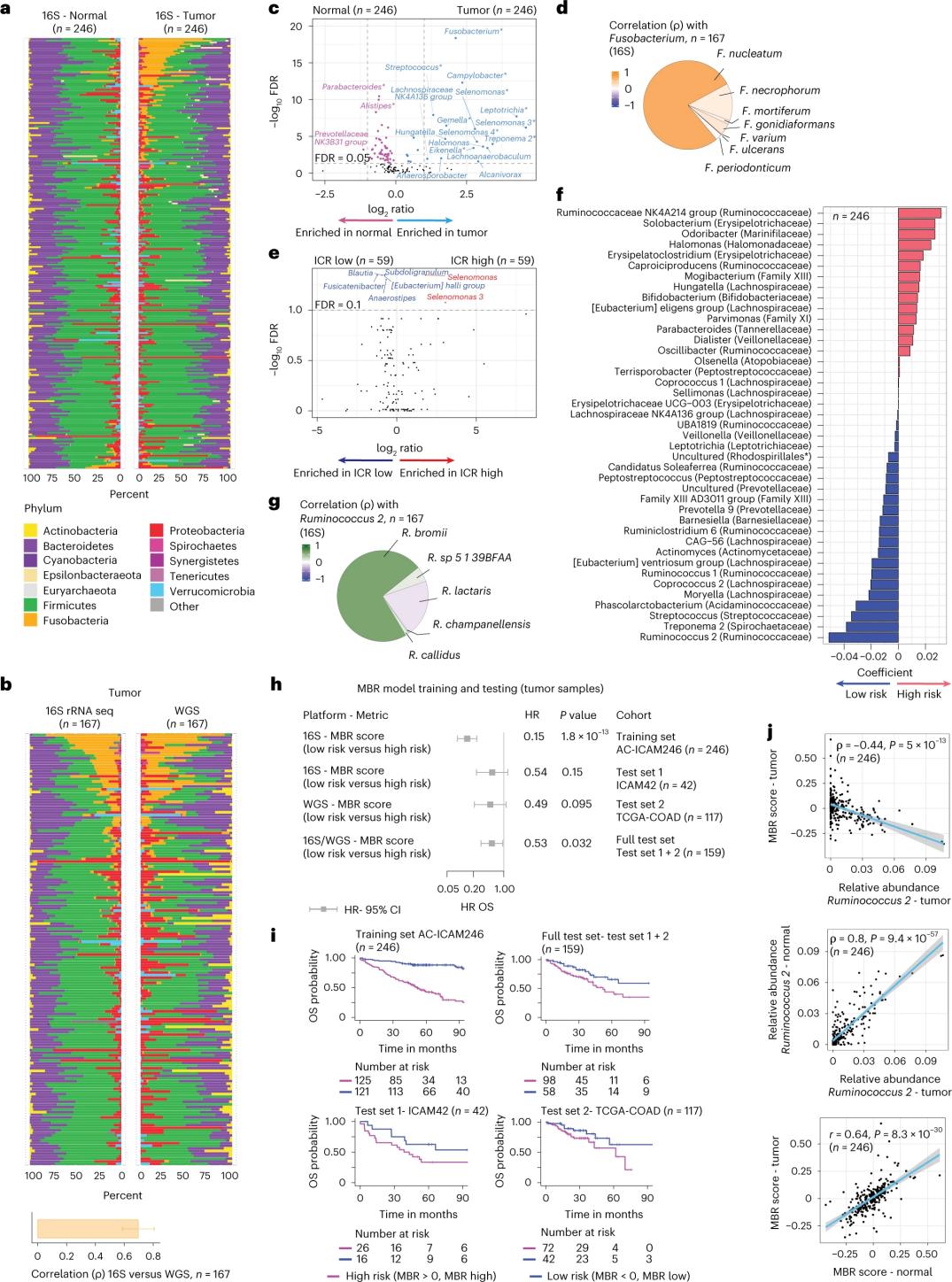
Joonis 3. Kasvaja ja tervete kudede mikrobioom ning seos infiltratsiooni ja patsiendi elulemusega.
Kokkuvõte
Selles uuringus kasutatud multioomiline lähenemisviis võimaldab kolorektaalvähi immuunvastuse molekulaarse signatuuri põhjalikku tuvastamist ja analüüsi ning paljastab mikrobioomi ja immuunsüsteemi interaktsiooni. Kasvaja ja tervete kudede sügav TCR-sekveneerimine näitas, et ICR-i prognostiline toime võib tuleneda selle võimest püüda kinni kasvajaga rikastatud ja võimalik, et ka kasvaja antigeenispetsiifilisi T-rakkude kloone.
Analüüsides kasvaja mikrobioomi koostist AC-ICAM proovides 16S rRNA geeni sekveneerimise abil, tuvastas meeskond mikrobioomi signatuuri (MBR riskiskoori), millel on tugev prognostiline väärtus. Kuigi see signatuur pärines kasvaja proovidest, oli terve kolorektumi ja kasvaja MBR riskiskoori vahel tugev korrelatsioon, mis viitab sellele, et see signatuur võib kajastada patsientide soole mikrobioomi koostist. ICR ja MBR skooride kombineerimise abil oli võimalik tuvastada ja valideerida multioomiline õpilaste biomarker, mis ennustab käärsoolevähiga patsientide ellujäämist. Uuringu multioomiline andmestik pakub ressurssi käärsoolevähi bioloogia paremaks mõistmiseks ja aitab avastada personaalseid ravimeetodeid.
Postituse aeg: 15. juuni 2023
 中文网站
中文网站