PCR-reaktsiooni käigus esineb sageli mõningaid segavaid tegureid.
PCR-i väga kõrge tundlikkuse tõttu peetakse saastumist üheks olulisemaks PCR-i tulemusi mõjutavaks teguriks ja see võib anda valepositiivseid tulemusi.
Samavõrd olulised on mitmesugused allikad, mis viivad vale-negatiivsete tulemusteni. Kui PCR-segu või amplifikatsioonireaktsiooni üks või mitu olulist osa on pärsitud või häiritud, võib diagnostiline analüüs olla takistatud. See võib viia efektiivsuse vähenemiseni ja isegi vale-negatiivsete tulemusteni.
Lisaks inhibeerimisele võib sihtnukleiinhappe terviklikkuse kadu tekkida transpordi- ja/või säilitamistingimuste tõttu enne proovi ettevalmistamist. Eelkõige võivad kõrged temperatuurid või ebapiisav säilitamine kahjustada rakke ja nukleiinhappeid. Rakkude ja kudede fikseerimine ning parafiini kinnistamine on DNA fragmentatsiooni tuntud põhjused ja püsiv probleem (vt joonised 1 ja 2). Sellistel juhtudel ei aita isegi optimaalne eraldamine ja puhastamine.
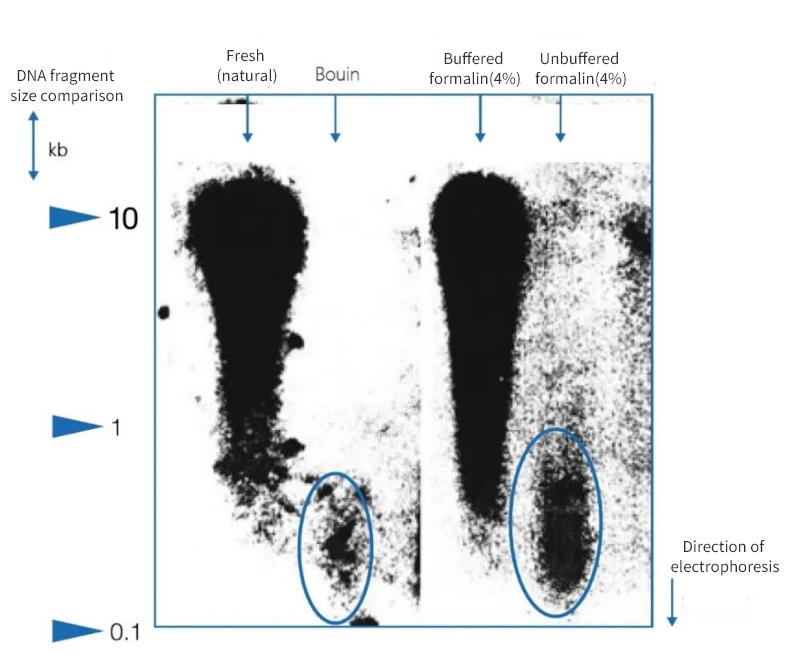
Joonis 1 | Immobiliseerimise mõju DNA terviklikkusele
Agaroosgeelelektroforees näitas, et lahkamiste parafiinilõikudest eraldatud DNA kvaliteet varieerus märkimisväärselt. Ekstraktides esines erineva keskmise fragmentide pikkusega DNA-d, olenevalt fikseerimismeetodist. DNA säilis ainult natiivsetes külmutatud proovides ja puhverdatud neutraalses formaliinis fikseerimisel. Tugevalt happelise Bouini fiksaatori või puhverdamata sipelghapet sisaldava formaliini kasutamine põhjustas DNA olulise kadumise. Ülejäänud fraktsioon on tugevalt fragmenteerunud.
Vasakul on fragmentide pikkus väljendatud kilobaasipaarides (kbp).
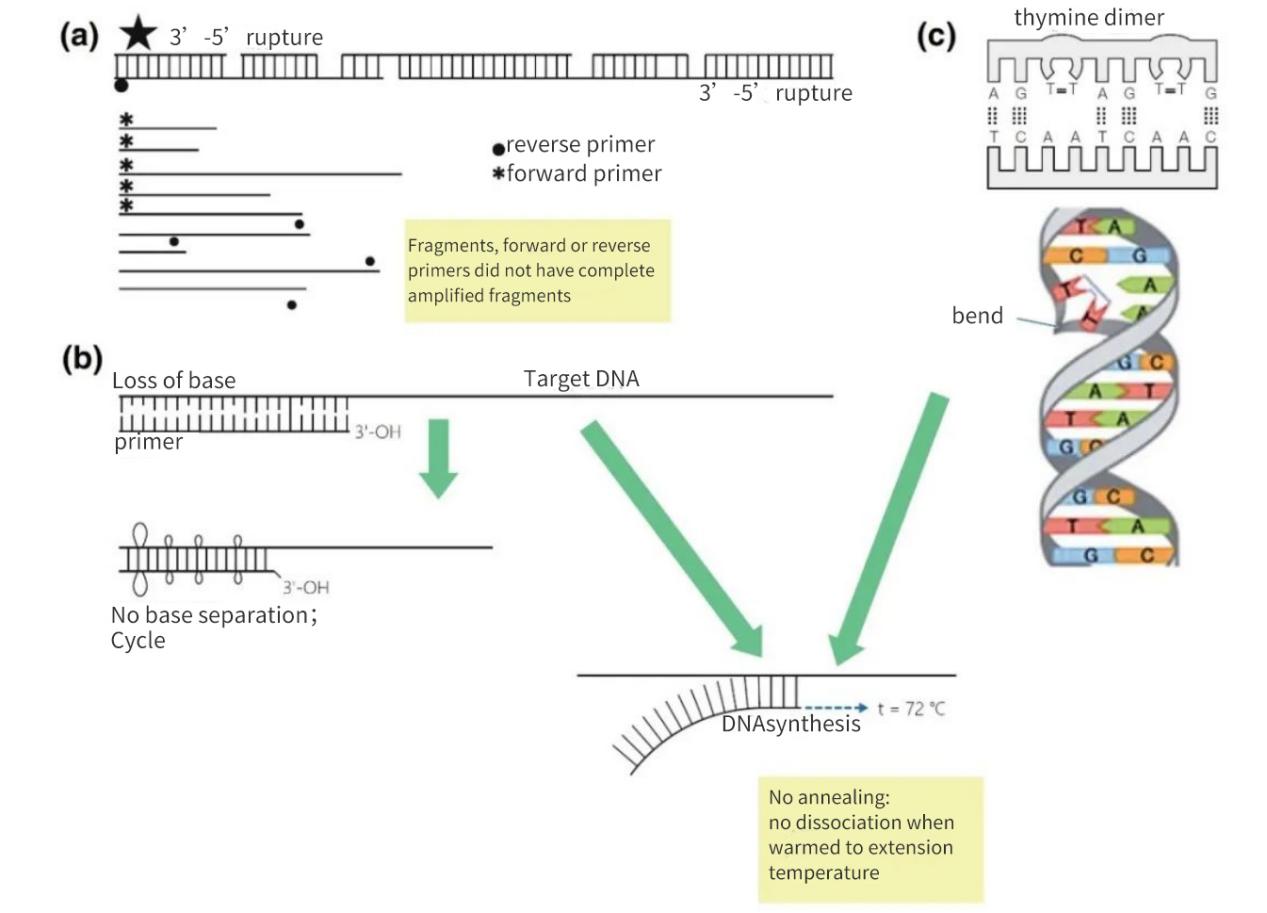
Joonis 2 | Nukleiinhappe sihtmärkide terviklikkuse kadu
(a) Mõlema ahela 3′-5′ tühimik põhjustab siht-DNA katkemise. DNA süntees toimub väikesel fragmendil ikkagi. Kui aga DNA fragmendil puudub praimeri anniilimiskoht, toimub ainult lineaarne amplifikatsioon. Kõige soodsamal juhul võivad fragmendid üksteist uuesti küllastada, kuid saagised on väikesed ja allapoole avastamispiiri.
(b) Aluste kadu, peamiselt depurinatsiooni ja tümidiini dimeeri moodustumise tõttu, viib H-sidemete arvu vähenemiseni ja Tm lühenemiseni. Pikenenud soojenemisfaasi ajal sulavad praimerid maatriks-DNA-st lahti ja ei anniilu isegi leebemates tingimustes.
(c) Kõrvutiasetsevad tümiini alused moodustavad TT-dimeeri.
Teine levinud probleem, mis molekulaardiagnostikas sageli esineb, on sihtnukleiinhapete ebapiisav vabanemine võrreldes fenooli-kloroformi ekstraheerimisega. Äärmuslikel juhtudel võib see olla seotud vale-negatiivsete tulemustega. Palju aega saab kokku hoida keetmislüüsi või rakujäätmete ensümaatilise lagundamise abil, kuid see meetod põhjustab sageli madalat PCR-tundlikkust ebapiisava nukleiinhapete vabanemise tõttu.
Polümeraasi aktiivsuse pärssimine amplifikatsiooni ajal
Üldiselt kasutatakse inhibeerimist konteinerikontseptsioonina, et kirjeldada kõiki tegureid, mis viivad optimaalsetest madalamate PCR-tulemusteni. Rangelt biokeemilisest mõttes piirdub inhibeerimine ensüümi aktiivsusega, st see vähendab või takistab substraadi muundumist produktiks interaktsiooni kaudu DNA polümeraasi või selle kofaktori aktiivse tsentriga (nt Mg2+ Taq DNA polümeraasi puhul).
Proovis olevad komponendid või mitmesugused puhvrid ja ekstraktid, mis sisaldavad reagente, võivad ensüümi otseselt pärssida või selle kofaktoreid (nt EDTA) püüda, inaktiveerides seeläbi polümeraasi ja omakorda põhjustades vähenenud või vale-negatiivseid PCR-tulemusi.
Siiski nimetatakse paljusid reaktsioonikomponentide ja sihtmärki sisaldavate nukleiinhapete vahelisi interaktsioone ka „PCR-i inhibiitoriteks“. Kui raku terviklikkus on isoleerimise teel häiritud ja nukleiinhape vabaneb, võivad tekkida interaktsioonid proovi ja selle ümbritseva lahuse ning tahke faasi vahel. Näiteks võivad „püüdjad“ siduda ühe- või kaheahelalise DNA mittekovalentsete interaktsioonide kaudu ning häirida isoleerimist ja puhastamist, vähendades sihtmärkide arvu, mis lõpuks PCR-i reaktsioonianumasse jõuavad.
Üldiselt leidub PCR-i inhibiitoreid enamikus kehavedelikes ja kliinilistes diagnostilistes testides kasutatavates reagentides (uurea uriinis, hemoglobiin ja hepariin veres), toidulisandites (orgaanilised komponendid, glükogeen, rasv, Ca2+ ioonid) ja keskkonna komponentides (fenoolid, raskmetallid).
| Inhibiitorid | Allikas |
| Kaltsiumiioonid | Piim, luukude |
| Kollageen | Kude |
| Sapphappe soolad | Väljaheited |
| Hemoglobiin | Veres |
| Hemoglobiin | Vereproovid |
| Humiinhape | Muld, taim |
| Veri | Veri |
| Laktoferriin | Veri |
| (Euroopa) melaniin | Nahk, juuksed |
| Müoglobiin | Lihaskude |
| Polüsahhariidid | Taim, väljaheited |
| Proteaas | Piim |
| Karbamiid | Uriin |
| Mukopolüsahhariid | Kõhr, limaskestad |
| Ligniin, tselluloos | Taimed |
Levinumaid PCR-i inhibiitoreid võib leida bakterites ja eukarüootsetes rakkudes, mitte-sihtmärk-DNA-s, koemaatriksite DNA-d siduvates makromolekulides ja laboriseadmetes, näiteks kinnastes ja plastides. PCR-i inhibiitorite eemaldamise eelistatud meetod on nukleiinhapete puhastamine ekstraheerimise ajal või pärast seda.
Tänapäeval saavad mitmesugused automatiseeritud ekstraheerimisseadmed asendada paljusid käsitsi tehtavaid protokolle, kuid sihtmärkide 100% taastumist ja/või puhastamist pole kunagi saavutatud. Puhastatud nukleiinhapetes võivad endiselt esineda potentsiaalsed inhibiitorid või need võivad olla juba mõju avaldanud. Inhibiitorite mõju vähendamiseks on olemas erinevad strateegiad. Sobiva polümeraasi valikul võib olla oluline mõju inhibiitori aktiivsusele. Teised tõestatud meetodid PCR-i inhibeerimise vähendamiseks on polümeraasi kontsentratsiooni suurendamine või lisandite, näiteks BSA, kasutamine.
PCR-reaktsioonide inhibeerimist saab demonstreerida sisemise protsessi kvaliteedikontrolli (IPC) abil.
Nukleiinhappe isolaadist tuleb hoolikalt pesta ja eemaldada kõik ekstraheerimiskomplektis olevad reagendid ja muud lahused, näiteks etanool, EDTA, CETAB, LiCl, GuSCN, SDS, isopropanool ja fenool. Sõltuvalt nende kontsentratsioonist võivad need PCR-i aktiveerida või pärssida.
Postituse aeg: 19. mai 2023
 中文网站
中文网站