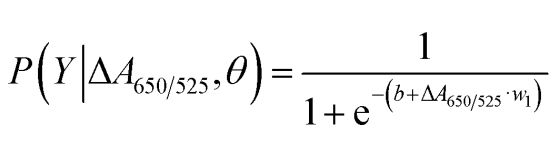Vähi varajane avastamine vedelbiopsia abil on uus vähi avastamise ja diagnoosimise suund, mille on viimastel aastatel välja pakkunud USA Riiklik Vähiinstituut, eesmärgiga avastada varajane vähk või isegi vähieelsed kahjustused. Seda on laialdaselt kasutatud uudse biomarkerina mitmesuguste pahaloomuliste kasvajate, sealhulgas kopsuvähi, seedetrakti kasvajate, glioomide ja günekoloogiliste kasvajate varajaseks diagnoosimiseks.
Metülatsioonimaastiku (Methylscape) biomarkerite tuvastamise platvormide teke võib oluliselt parandada olemasolevat vähi varajast sõeluuringut, viies patsiendid varaseimasse ravitavasse staadiumisse.
Hiljuti on teadlased välja töötanud lihtsa ja otsese tuvastamise platvormi metülatsioonimaastiku tuvastamiseks, mis põhineb tsüsteamiiniga kaunistatud kulla nanoosakestel (Cyst/AuNP-d) koos nutitelefonipõhise biosensoriga, mis võimaldab laia valiku kasvajate kiiret ja varajast skriinimist. Leukeemia varajast skriinimist saab teha 15 minuti jooksul pärast DNA ekstraheerimist vereproovist, täpsusega 90,0%. Artikli pealkiri on "Vähi DNA kiire tuvastamine inimese veres, kasutades tsüsteamiiniga kaunistatud AuNP-sid ja masinõppega nutitelefoni".
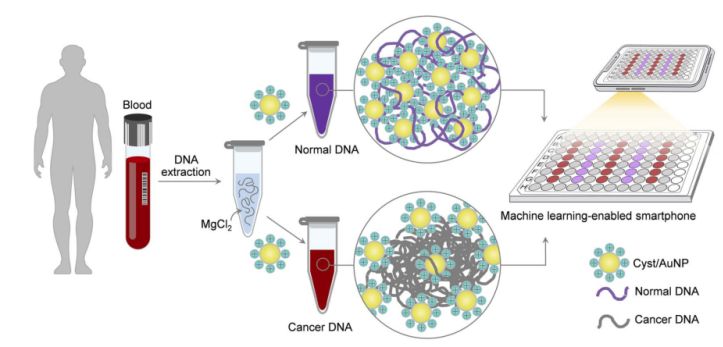
Joonis 1. Cyst/AuNP-de komponentide abil vähi sõeluuringute lihtsa ja kiire tuvastamisplatvormi saab luua kahes lihtsas etapis.
See on näidatud joonisel 1. Esmalt kasutati DNA fragmentide lahustamiseks vesilahust. Seejärel lisati segatud lahusele tsüst/AuNP-d. Normaalsel ja pahaloomulisel DNA-l on erinevad metüleerimisomadused, mille tulemuseks on DNA fragmendid, millel on erinevad iseassambleerumismustrid. Normaalne DNA agregeerub lõdvalt ja lõpuks agregeerib tsüst/AuNP-sid, mille tulemuseks on tsüst/AuNP-de punanihkumine, nii et värvuse muutus punasest lillaks on palja silmaga jälgitav. Seevastu vähi DNA ainulaadne metüleerimisprofiil viib suuremate DNA fragmentide klastrite tekkeni.
96-auguliste plaatide pildid jäädvustati nutitelefoni kaameraga. Vähi DNA-d mõõdeti masinõppega varustatud nutitelefoniga, võrreldes spektroskoopiapõhiste meetoditega.
Vähi sõeluuring päris vereproovides
Sensorplatvormi kasulikkuse laiendamiseks rakendasid uurijad andurit, mis eristas edukalt normaalset ja vähi DNA-d reaalsetes vereproovides. CpG saitide metülatsioonimustrid reguleerivad epigeneetiliselt geeniekspressiooni. Peaaegu kõigi vähitüüpide puhul on täheldatud DNA metülatsiooni ja seega ka tuumorigeneesi soodustavate geenide ekspressiooni muutuste vaheldumist.
DNA metülatsiooniga seotud teiste vähivormide mudelina kasutasid teadlased leukeemiahaigete ja tervete kontrollisikute vereproove, et uurida metülatsioonimaastiku efektiivsust leukeemiliste vähkide eristamisel. See metülatsioonimaastiku biomarker mitte ainult ei ületa olemasolevaid kiireid leukeemia sõeluuringu meetodeid, vaid näitab ka selle lihtsa ja otsekohese testi abil laia vähivormide varajase avastamise teostatavust.
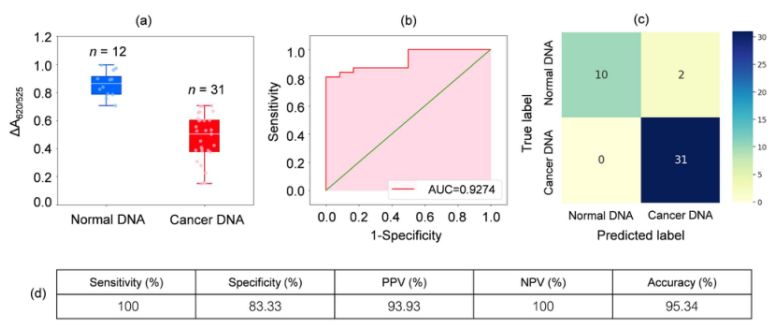
Analüüsiti 31 leukeemiahaige ja 12 terve inimese vereproovidest võetud DNA-d. Nagu joonisel 2a oleval kastidiagrammil näidatud, oli vähiproovide suhteline neelduvus (ΔA650/525) madalam kui normaalsete proovide DNA-l. See oli peamiselt tingitud suurenenud hüdrofoobsusest, mis viis vähi DNA tiheda agregatsioonini, mis takistas tsüst/AuNP-de agregatsiooni. Selle tulemusena olid need nanoosakesed täielikult hajutatud vähi agregaatide väliskihtidesse, mille tulemuseks oli normaalsetele ja vähi DNA agregaatidele adsorbeerunud tsüst/AuNP-de erinev hajumine. Seejärel genereeriti ROC-kõverad, varieerides läve minimaalsest väärtusest ΔA650/525 maksimaalse väärtuseni.
Joonis 2. (a) Tsüstide/AuNP-de lahuste suhtelise neeldumise väärtused, mis näitavad normaalse (sinine) ja vähi (punane) DNA olemasolu optimeeritud tingimustes
(b) kastidiagrammide (DA650/525) analüüs; (b) diagnostiliste testide ROC-analüüs ja hindamine. (c) normaalsete ja vähihaigete diagnoosimise segamismaatriks. (d) väljatöötatud meetodi tundlikkus, spetsiifilisus, positiivne ennustusväärtus (PPV), negatiivne ennustusväärtus (NPV) ja täpsus.
Nagu joonisel 2b näidatud, näitas väljatöötatud sensori ROC-kõvera alune pindala (AUC = 0,9274) suurt tundlikkust ja spetsiifilisust. Nagu kastidiagrammilt näha, ei ole normaalse DNA rühma esindav madalaim punkt vähi DNA rühma esindavast kõrgeimast punktist hästi eraldatud; seetõttu kasutati normaalse ja vähi rühma eristamiseks logistilist regressiooni. Arvestades sõltumatute muutujate komplekti, hindab see sündmuse, näiteks vähi või normaalse rühma, toimumise tõenäosust. Sõltuv muutuja jääb vahemikku 0 kuni 1. Tulemuseks on seega tõenäosus. Vähi tuvastamise tõenäosuse (P) määrasime ΔA650/525 põhjal järgmiselt.
kus b=5,3533, w1=-6,965. Proovi klassifitseerimise puhul näitab tõenäosus alla 0,5 normaalset proovi, samas kui tõenäosus 0,5 või suurem näitab vähiproovi. Joonis 2c kujutab segamismaatriksit, mis genereeriti ristvalideerimise teel, mida kasutati klassifitseerimismeetodi stabiilsuse valideerimiseks. Joonis 2d võtab kokku meetodi diagnostilise testi hindamise, sealhulgas tundlikkuse, spetsiifilisuse, positiivse ennustusväärtuse (PPV) ja negatiivse ennustusväärtuse (NPV).
Nutitelefonipõhised biosensorid
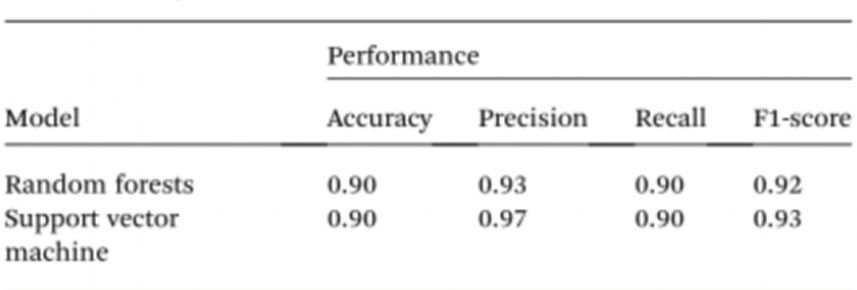
Spektrofotomeetriteta proovide testimise edasiseks lihtsustamiseks kasutasid teadlased tehisintellekti (AI), et tõlgendada lahuse värvi ja eristada normaalseid ning vähihaigeid. Seda arvestades kasutati arvutinägemist, et teisendada tsüst/AuNP-de lahuse värv normaalseks DNA-ks (lilla) või vähihaige DNA-ks (punane), kasutades mobiiltelefoni kaameraga tehtud 96-süvendiliste plaatide pilte. Tehisintellekt aitab vähendada kulusid ja parandada nanoosakeste lahuste värvi tõlgendamise kättesaadavust ilma nutitelefoni optiliste riistvaraliste lisaseadmeteta. Lõpuks treeniti mudelite loomiseks kahte masinõppe mudelit, sealhulgas Random Forest (RF) ja Support Vector Machine (SVM). Nii RF- kui ka SVM-mudelid klassifitseerisid proovid õigesti positiivseteks ja negatiivseteks 90,0% täpsusega. See viitab sellele, et tehisintellekti kasutamine mobiiltelefonipõhises biosensoris on täiesti võimalik.
Joonis 3. (a) Proovi ettevalmistamise ajal pildistamise etapis registreeritud lahuse sihtklass. (b) Pildi pildistamise etapis tehtud näidispilt. (c) Pildilt (b) eraldatud tsüsti/AuNP-de lahuse värvuse intensiivsus 96-süvendilise plaadi igas süvendis.
Kasutades tsüst/AuNP-sid, on teadlased edukalt välja töötanud lihtsa sensorplatvormi metülatsioonimaastiku tuvastamiseks ja anduri, mis suudab eristada normaalset DNA-d vähi DNA-st, kui leukeemia skriinimiseks kasutatakse päris vereproove. Väljatöötatud andur näitas, et päris vereproovidest ekstraheeritud DNA suutis leukeemiapatsientidel kiiresti ja kulutõhusalt tuvastada väikeseid koguseid vähi DNA-d (3nM) 15 minutiga ning näitas täpsust 95,3%. Proovide testimise edasiseks lihtsustamiseks spektrofotomeetri vajaduse kaotamise teel kasutati masinõpet lahuse värvi tõlgendamiseks ja normaalsete ja vähihaigete eristamiseks mobiiltelefonifoto abil ning täpsus saavutati samuti 90,0%.
Viide: DOI: 10.1039/d2ra05725e
Postituse aeg: 18. veebruar 2023
 中文网站
中文网站